近日,中国海洋大学医药学院、海洋药物教育部重点实验室、青岛海洋科技中心海洋药物与生物制品功能实验室王杨教授课题组在环状亚胺的不对称催化亲核加成反应合成β-咔啉类化合物方面取得重要进展。相关研究成果以“Asymmetric catalytic construction of β-carbolines via nucleophilic addition of silylenol ethers with cyclic imines(通过烯醇硅醚与环状亚胺的亲核加成反应实现β -咔啉的不对称催化合成)”为题,发表在Chinese Chemical Letters期刊上。
C1位取代的β -咔啉结构广泛存在于多种天然产物和具有生物活性的化合物中,具有多样的药理学特性(图1a)。在对C1位取代的β -咔啉结构的多种合成方法中,对环状亚胺或亚胺鎓进行不对称亲核加成已成为构建这一重要骨架最高效的方法之一。尽管该策略已成功应用于酮类、烯酮类、氮杂内酯类、吲哚类及硼烷类作为亲核试剂,但开发替代性亲核试剂仍极具必要性,可以拓展β -咔啉衍生物的结构多样性。现有的烯醇硅醚与环状亚胺的不对称亲核加成反应仅通过手性底物或手性助剂进行,且其对映选择性仅处于中等水平,后续还需额外步骤去除手性助剂,导致原子利用率较低。为此,王杨教授课题组利用一种新型阴离子结合的催化模式,实现了烯醇硅醚与亚胺之间的不对称催化亲核加成反应,以此为基础构建了一系列结构多样的高对映选择性C1位取代β -咔啉衍生物(图1b)。该反应模式具有广泛的底物范围以及高的产率和对映选择性。
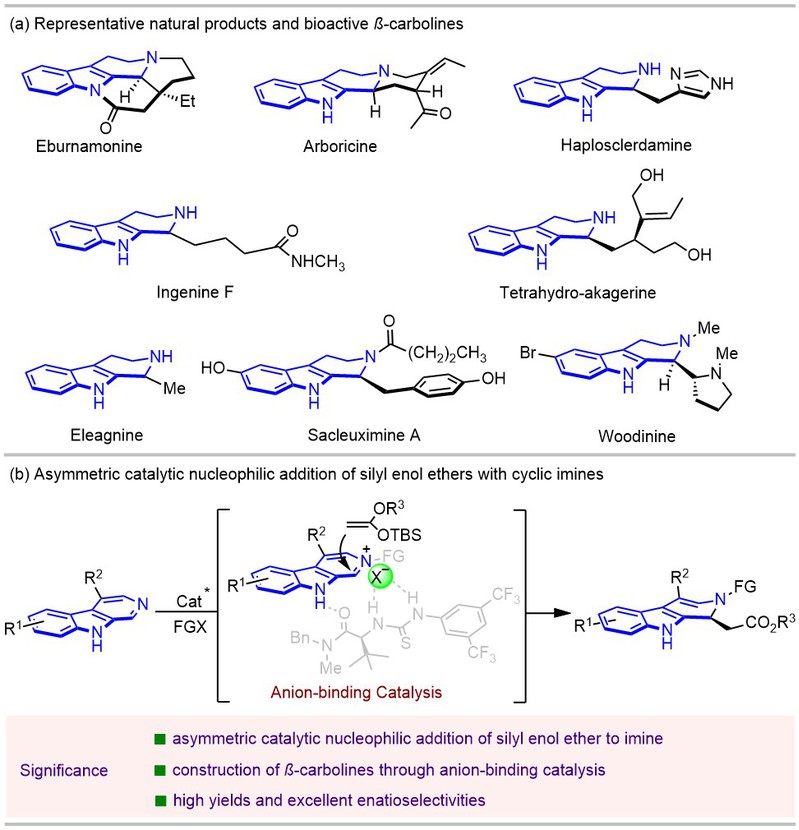
图1 代表性天然产物与通过烯醇硅醚与亚胺不对称合成C1位取代的β-咔啉
在确定了最佳反应条件后,作者对该方法的普适性进行了考察(图2a)。结果显示,在5位、6位和7位被取代的环状亚胺(包括供电子基团和吸电子基团)均表现出良好的耐受性,成功以高产率和优异的对映选择性获得了产物。然而,8-甲氧基取代的环状亚胺对映选择性较低,这可能是由于空间位阻影响了催化剂与底物的相互作用。该反应对4-甲基和苄基取代的底物也表现出良好耐受性,以中等产率获得了对映选择性良好至优异的产物。对亲核试剂的进一步研究显示,带有乙基、苄基和叔丁基的烯醇硅醚均能耐受,以高对映选择性得到对应的目标产物。为验证该反应体系的实用价值,作者对其合成应用进行了系统探究(图2b)。在三乙基硅氢和TFA作用下,化合物3a以95%的产率被还原为化合物4a,且对映纯度未发生任何损失。随后对Troc基团进行脱保护,以88%的产率得到未保护的β-咔啉化合物5a,对映选择性得以保持。值得注意的是,该不对称合成方法的实用性通过将产物3s转化为化合物5b得到了进一步验证。化合物5b是合成具有生物活性的canthin-5,6-二酮生物碱的关键中间体。借助化合物5b,一步合成路线可便捷获得先前报道的关键中间体6a、6b和6c—这些多用途前体可用于合成多种天然产物,包括(−)-harmicine、(−)-yohimbone、(−)-yohimbol、(−)-alloyohimbone、(−)-17-epiyohimbol、(−)-arboricine和(−)-geissoschizol。
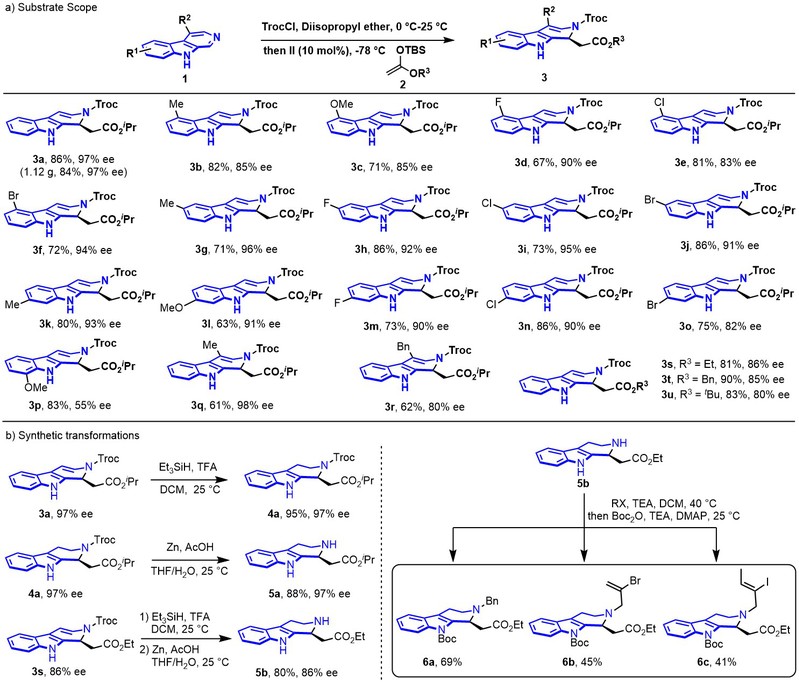
图2 底物拓展、产物衍生化及合成天然产物关键中间体
本文的第一完成单位是中国海洋大学医药学院,王杨教授为通讯作者。该工作得到了国家自然科学基金、泰山学者青年专家等项目的支持。
文章链接:https://www.sciencedirect.com/science/article/pii/S1001841726004389
【关闭】





