近日,中国海洋大学医药学院、海洋药物教育部重点实验室王洪玉教授联合中国科学院上海有机化学研究所赵刚研究员,在自由基不对称催化有机合成领域取得重要进展。相关研究成果以“Copper-Photocatalyzed Enantioselective S-Alkylation of Sulfenamides Enabled by Amino-Acid-Derived N,N,N-Tridentate Ligand”(氨基酸衍生的N,N,N三齿配体诱导铜/光协同不对称催化次磺酰胺对映选择性S-烷基化反应)为题,发表在国际知名学术期刊ACS Catalysis.(DOI: 10.1021/acscatal.6c01852)上。
生物电子等排体替换已成为药物化学中优化候选药物理化性质的重要策略。在众多突出进展中,凭借sulfoximines独特的理化属性(如弱碱性、高化学稳定性与代谢稳定性、适宜极性等),用其替代砜基的策略日益受到关注。手性sulfilimines是药物化学中具有重要价值的含硫手性结构单元,同时也是构建sulfoximines和sulfondiimines的多功能前体。尽管其重要性不言而喻,但通过对sulfenamides进行不对称S-烷基化的反应却研究不足。
我们报道了一种由氨基酸衍生的N,N,N三齿配体促进的铜/光氧化还原协同催化不对称S-烷基化反应。该策略通过脱羧自由基亚磺亚胺化过程,实现了烷基羧酸作为烷基自由基前体的高效利用,从而以优异的产率和对映选择性获得手性富集的亚磺亚胺产物。值得注意的是,该反应体系还可拓展至烷基碘化物底物,通过XAT(卤原子转移)诱导的自由基路径实现转化,体现了该不对称S-烷基化策略的良好通用性。该方法对一级、二级及三级烷基自由基、不同类型的硫代酰胺底物以及复杂生物活性分子均表现出良好的兼容性。并实现了多个生物活性分子中间体的高效合成。此外,克级规模反应及后续氧化转化为具有药物相关性的亚砜亚胺,进一步凸显了该方法在药物化学中的应用价值。
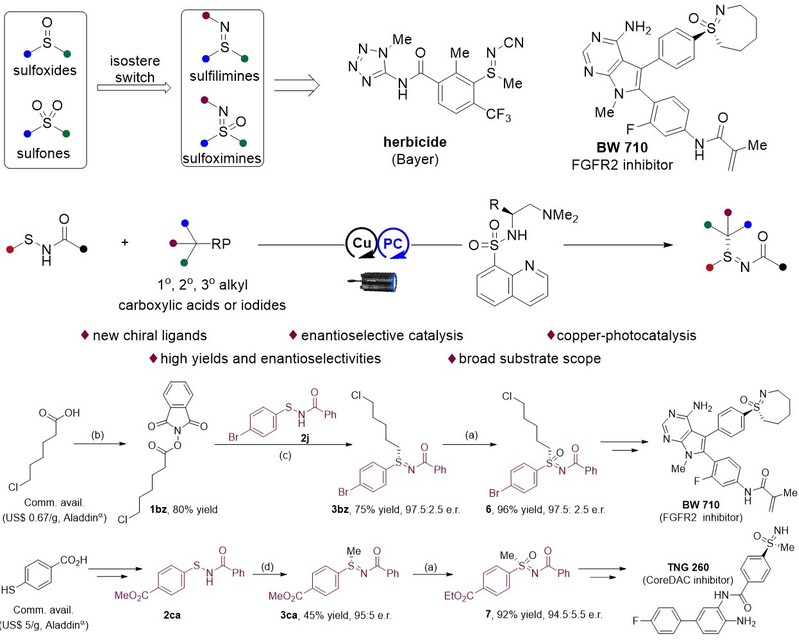
图1 不对称S-烷基化反应
研究成果发表于国际知名期刊《ACS Catalysis》(中科院一区,Top期刊,影响因子13.1)。中国海洋大学医药学院为第一通讯单位,中国海洋大学医药学院王洪玉教授与上海有机化学研究所赵刚研究员为共同通讯作者,医药学院博士研究生庄相玉和硕士研究生孙笑为共同第一作者。研究工作得到了国家自然科学基金、泰山学者青年专家、山东省自然科学基金、中国海洋大学青年英才启动经费等项目资助。
文章链接:https://pubs.acs.org/doi/10.1021/acscatal.6c01852
【关闭】





