近日,中国海洋大学医药学院、海洋药物教育部重点实验室李德海教授联合王伟教授,在人工智能驱动的药物分子生成领域取得重要进展,实现了方法学创新以及完整应用生态的构建,完成了从算法到验证的闭环。该研究在国际知名学术期刊Journal of Medicinal Chemistry在线发表题为《Pocket-based generative diffusion model accelerates potent influenza A hemagglutinin inhibitor discovery(基于口袋的生成式扩散模型加速强效甲型流感血凝素抑制剂的发现)》的研究文章(doi: 10.1021/acs.jmedchem.5c03787)。
传统的创新药物发现流程漫长,人工智能的应用则极大提升了研发效率。尽管新型AI生成模型不断被报道,但仍存在多种局限,包括:(1)现有研究通常将蛋白结合口袋信息直接输入模型进行训练,未能充分利用蛋白口袋的结构特征。(2)仅学习蛋白质-配体联合分布无法有效区分最优与次优结合构象,对生成高亲和力分子的指导不足,且现有生成模型的可解释性通常不足。(3)现有模型所生成分子的生物活性效能依然不理想,制约了实际应用。
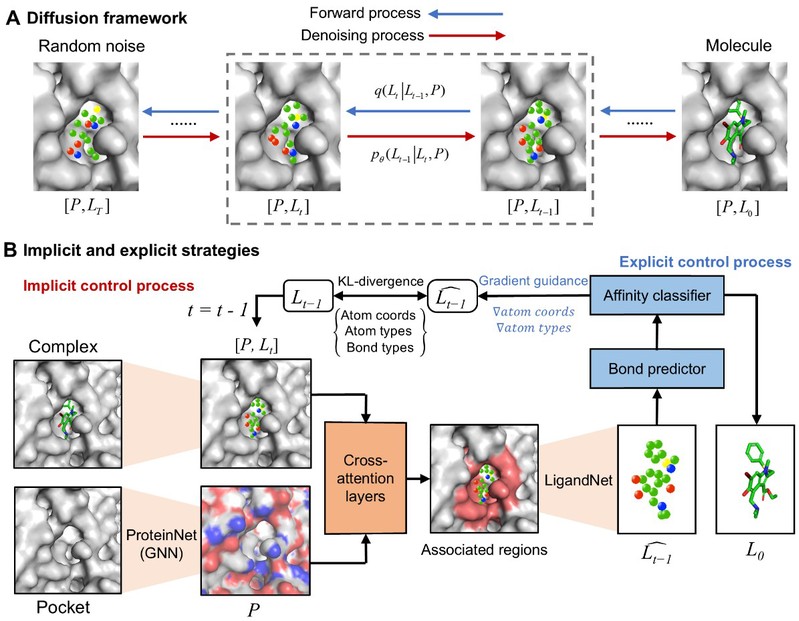
图1. 基于口袋的生成式扩散模型用于强效甲型流感血凝素抑制剂的发现
为了解决以上局限,研究团队创新性的开发了“隐式+显式”双控制扩散模型(DCDM,图1)以增强3D口袋感知的分子生成。该模型以Diffusion扩散模型为基础,利用加噪/去噪的方式构建3D原子结构,并利用共价键预测器预测键的类型;进而通过图神经网络提取蛋白信息,与配体信息通过注意力机制隐式控制整合,强调与配体最相关的口袋部分;以Vina打分为指标训练亲和力分类器,以预测复合物中原子的亲和力,显式控制进行生成后指导,引导模型朝亲和力增加的方向生成分子。在采用测试数据集进行的模型测试中,团队开发的DCDM模型与其它主流分子生成模型相比,其生成的分子具有更强的亲和力打分,且生成的分子结构合理、结构多样。并且DCDM能够准确识别蛋白潜在结合位点,原子贡献打分与药物化学知识较好匹配,证明了模型具有良好的可解释性和可靠性(图2)。
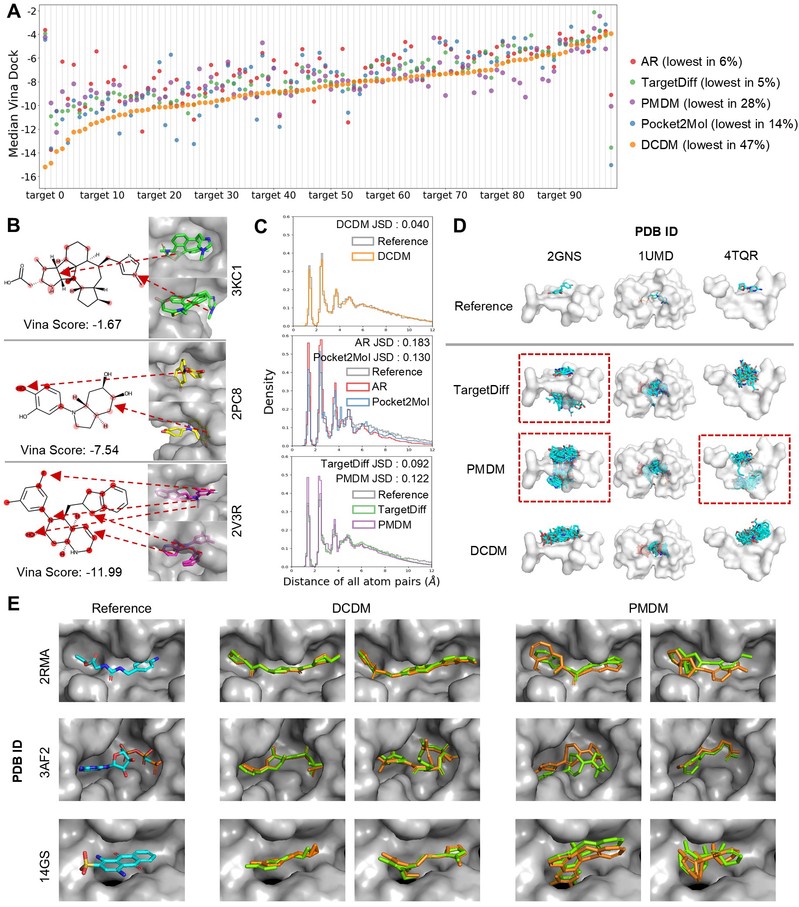
图2. AI驱动药物设计模型的良好可解释性和可靠性
进而利用DCDM模型对前期发现的抗流感先导化合物PND进行了优化。PND是团队从南极海洋真菌中发现的新结构代谢产物,其靶向甲型流感血凝素(HA)蛋白发挥抗病毒作用(J. Med. Chem.2020, 63, 6924.)。团队前期通过分子对接及传统药物化学策略设计合成60余个新型衍生物(Eur. J. Med. Chem. 2023, 258, 115615.),初步探讨了其构效关系。后续深入研究发现PND潜在结合位点较浅且柔性较大,运用传统策略的优化效率较低。因此本研究中团队运用DCDM模型进行新一代PND结构优化工作。通过DCDM固定位点生成了11,000余个新分子,经QED、SA和Vina Dock打分筛选得到502个新分子,最后经目视检查最终选择合成3类结构多样的化合物,包括苯衍生物、醚类/酰胺类化合物,其连接长度不同表明其在结合口袋中可能占据不同的空间区域。经DCDM推荐合成的3个新型衍生物对HA蛋白的亲和力及均有不同程度的提升。进一步进行结构优化共合成5个衍生物,从中得到最优候选化合物C2e,其对HA蛋白的亲和力提高至约为母体化合物PND的26倍,体外抗病毒IC50约为PND的10倍。进一步药理学研究表明,C2e具有广谱抗甲型流感病毒活性,且能够抑制HA介导的合胞体形成。内体实验表明,C2e能够起到保护感染H1N1小鼠的作用,效果几乎与巴洛沙韦相当,且显著高于PND。初步毒性实验与药代动力学实验证明其具有良好的成药潜力。本研究结合DCDM模型仅合成8个新型衍生分子便可获得优于先导的化合物C2e,药物发现效率提升,验证了DCDM生成模型在加速真实世界药物开发方面的实用价值,为人工智能驱动的新药发现提供了新范式(图3)。
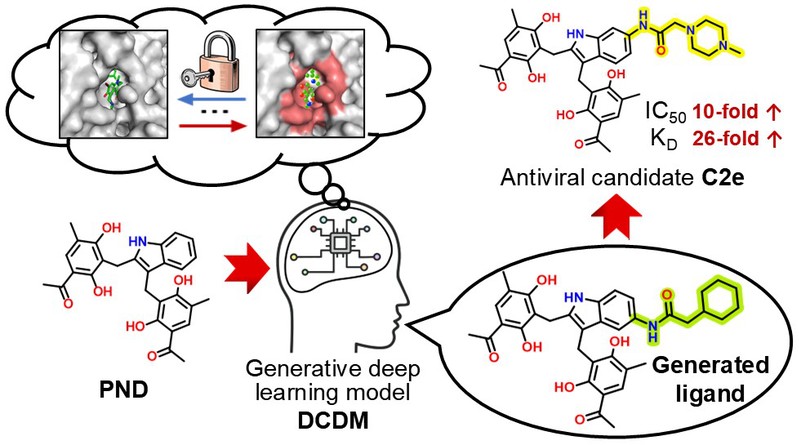
图3. 人工智能驱动新药发现的新范式
本文的第一完成单位是中国海洋大学,通讯作者为李德海教授与王伟教授。文章第一作者(含共同)是医药学院博士生盖文睿、吴双以及医药学院毕业生李博涵博士、张洋博士。上述工作得到了海南省重点研发项目、国家自然科学基金、青岛海洋科技中心科技创新项目、山东省泰山学者特聘专家等项目的支持。
文章链接:
https://doi.org/10.1021/acs.jmedchem.5c03787
参考文献:
https://doi.org/10.1016/j.ejmech.2023.115615
https://dx.doi.org/10.1021/acs.jmedchem.0c00312
【关闭】





