铁死亡是近年来定义的一种新型细胞死亡形式,其特征是由于不受限制的脂质过氧化和随后的膜损伤导致的铁依赖性细胞死亡。越来越多的研究表明,铁死亡在肿瘤、神经退行性疾病和组织缺血再灌注损伤等病理过程中发挥着重要作用。谷胱甘肽过氧化物酶4(Glutathione peroxidase 4, GPX4)是细胞铁死亡的关键靶点,经药物治疗的肿瘤细胞耐药株的生存高度依赖GPX4,因此GPX4抑制剂被视为解决肿瘤耐药问题的重要途径。但GPX4的活性位点附近结构相对扁平,是一个较难成药的靶点,开发GPX4的小分子抑制剂具有非常大的挑战。目前GPX4的小分子抑制剂大多存在生物利用度低、选择性较差等问题,亟需开发新型GPX4抑制剂。近日,中国海洋大学医药学院邱雪课题组与合作者在化学综合性期刊《Chemical Science》发表了一篇题为“A Potent and Selective Anti-Glutathione Peroxidase 4 Nanobody as Ferroptosis Inducer”的研究论文,开发了一种可以通过靶向GPX4诱导肿瘤细胞发生铁死亡的纳米抗体,显示了其在抗肿瘤治疗方面的应用潜力。
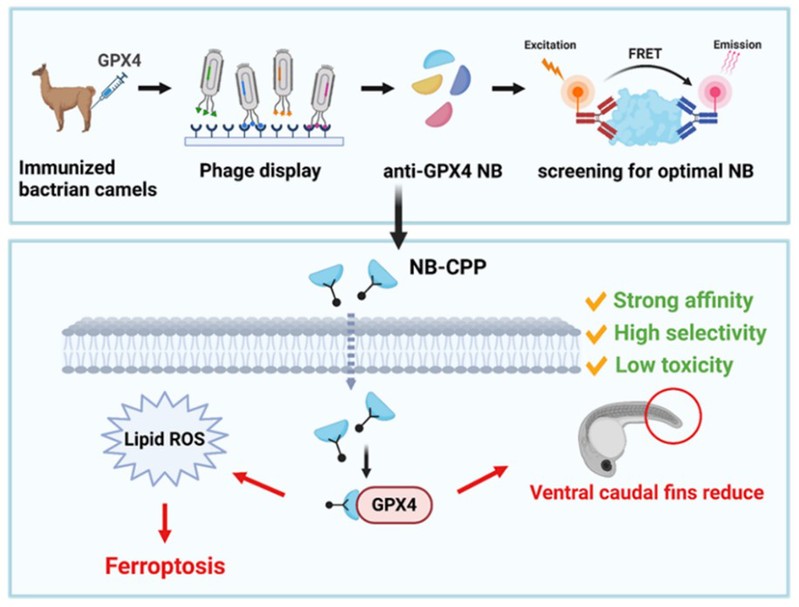
图1.纳米抗体的制备及其诱导细胞铁死亡的示意图
该研究利用GPX4重组蛋白免疫双峰驼,构建噬菌体文库制备靶向GPX4纳米抗体,利用荧光共振能量转移和表面等离子共振等多种分析技术高效筛选具有对GPX4高亲和力纳米抗体,利用细胞穿膜肽作为辅助手段,在细胞水平筛选具有诱导细胞铁死亡活性的纳米抗体。其中纳米抗体12E具有较强的细胞铁死亡诱导活性(IC50=0.56 μM),同时可以被铁死亡抑制剂Fer-1逆转,对正常细胞毒性较小,表现出良好的选择性。分子对接、分子动力学模拟以及GPX4突变体和12E的亲和力的测定结果均显示,12E特异性结合在GPX4的活性位点,通过正构调节直接抑制GPX4活性。在使用12E-R10进行细胞水平的铁死亡相关生物学指标检测过程中发现,12E-R10孵育细胞后,胞内的丙二醛(MDA)和前列腺素合成酶2(PTGS2)mRNA水平均显著升高。除此之外,12E-R10可以明显抑制外源GPX4WT的活性,这进一步验证了12E具有诱导细胞铁死亡的活性。(图2)
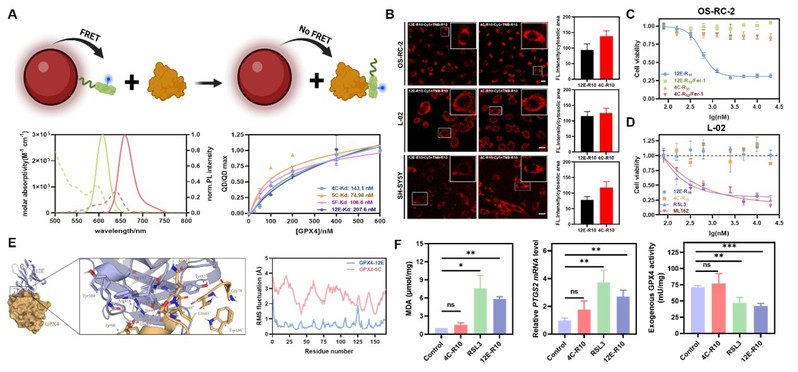
图2.分子及细胞水平相关实验。
除此之外,12E在斑马鱼体内表现出靶向GPX4的高灵敏度和专一性以及良好的安全性,突显了纳米抗体在GPX4相关机制研究和药物开发的巨大潜力,也为传统上难以治疗的靶点药物提供了新的纳米抗体研究范例。中国海洋大学医药学院为本文的第一通讯单位,中国海洋大学邱雪教授、王勇教授、华南农业大学徐振林教授为共同通讯作者,中国海洋大学医药学院博士研究生李鑫雨为第一作者,该研究也得到了中国海洋大学徐锡明、周建峰教授的大力支持。本工作得到了青岛海洋科技中心科技创新项目,山东省泰山学者青年专家项目、山东省优青、国家自然基金青年科学基金等项目的资助。
原文链接:https://doi.org/10.1039/d4sc05448b
【关闭】





