糖聚合物因其可以模拟天然多糖的结构特征及生物学功能,在生物医学领域展现了重要的应用价值。然而,传统糖聚合物的两亲性导致其在水溶液中自组装形成纳米胶束,影响了其与靶标蛋白的分子识别能力。因此,精确调控糖聚合物的自组装行为是其充分发挥生物学活性的关键。
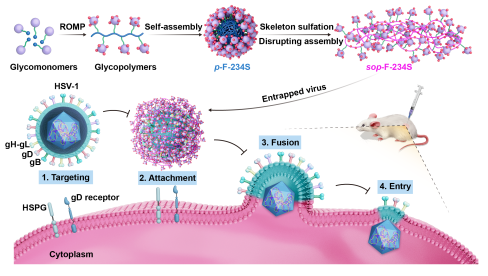
图1. 岩藻聚糖模拟物抗HSV-1的作用机制
中国海洋大学医药学院蔡超教授、王伟教授和于广利教授共同合作,采用烯烃复分解开环聚合反应(ROMP)策略设计合成了具有抗I型抗单纯疱疹病毒(HSV-1)作用的岩藻糖化聚合物。研究人员通过氢化还原获得了饱和C-C单键骨架的聚合物(hp-F-0S/234S)、双羟基骨架的聚合物(op-F-0S/234S),以及硫酸化修饰的聚阴离子糖骨架聚合物(sop-F-234S,图2),并利用TEM、AFM等技术对系列岩藻糖基聚合物的高级结构及理化性质进行了分析,发现骨架修饰可显著影响聚合物的自组装行为并调控其高级结构特征。值得注意的是,骨架硫酸化修饰的岩藻糖聚合物(sop-F-234S)表现出了柔性的线性结构,能破坏聚合物的自组装结构,形成与天然岩藻多糖相似的非组装形态(图3)。在体外、体内的抗HSV-1研究中,具有柔性线性结构的聚合物sop-F-234S抑制HSV-1感染的效果最好,不仅优于未修饰的岩藻糖聚合物,更超越了天然岩藻聚糖。机制研究表明,这些岩藻糖基聚合物通过靶向病毒胞膜蛋白gB、gD和gH/gL,有效阻断病毒侵入宿主细胞的过程(图1)。这一发现为糖聚合物骨架的理性设计提供了重要理论依据。相关研究成果以“Synthesis of Fucoidan-BiomimeticGlycopolymers with Flexible Skeletons forEnhanced Anti-Herpes Virus Efficacy”为题发表于《ACS Nano》。文章第一作者是中国海洋大学医药学院张萍博士和闫涵博士,该研究得到国家自然科学基金等多个项目支持。
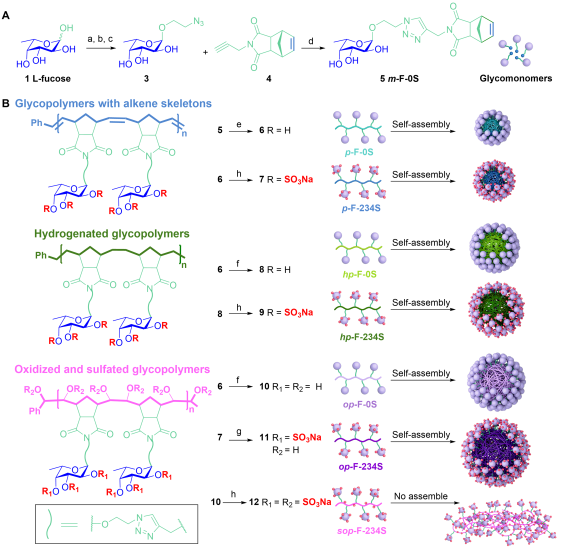
图2. 骨架修饰岩藻糖聚合物的合成方法
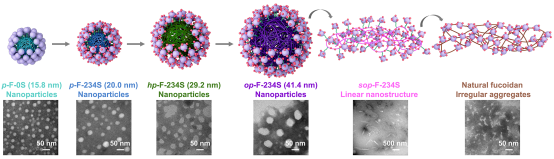
图3. 利用TEM分析不同骨架修饰岩藻糖基聚合物的纳米结构
糖聚合物的高级结构及功能不仅受聚合物骨架的化学修饰调控,糖基侧链的结构特征同样是决定其生物活性的关键因素。基于此,团队采用ROMP合成了同时含有硫酸化岩藻糖和6'-唾液酸乳糖的杂合型糖聚合物。该聚合物能够发挥双靶向作用,能同时靶向甲型流感病毒(IAV)表面的血凝素(HA)和神经氨酸酶(NA),实现对病毒“入侵”和“释放”致病周期的双阻断。值得关注的是,该双靶向抑制剂展现了广谱抗病毒特性,对多种亚型的HINI、H3N2耐药突变株均具有显著抑制效果。构效关系研究表明,糖配体密度、连接臂长度及配体比例是调控其抗IAV 活性的关键结构参数(ACS Macro Lett. 2024, 13, 874-881. ACS Macro Lett. 2025,doi: 10.1021/acsmacrolett.5c00121.)。上述系列研究为开发新型抗病毒糖基聚合物药物提供了重要的理论支撑。
原文链接:https://doi.org/10.1021/acsnano.4c15060
https://pubs.acs.org/doi/10.1021/acsmacrolett.4c00221
【关闭】





