纳米药物肿瘤靶向效率低,抗体免疫药物因肿瘤微环境的复杂性—激活的T细胞易“疲劳”,难以到达肿瘤免疫缺陷微区等因素导致患者响应率低。针对此情况,中国海洋大学医药学院王成副教授团队构建了一种兼具化疗和免疫疗法双重抗肿瘤特性的纳米小分子免疫激活剂(I3A-PM)(Ingenol-3-Mebutate,简称I3A,为大戟科植物汁液中提取的主要活性物质;体外研究表明,I3A具有较好抗肿瘤活性,但由于其疏水性、pH-不稳定性和毒性,极大地阻碍了其临床应用。I3A全身给药治疗深层肿瘤及体内抑瘤机制之前未有研究报道)
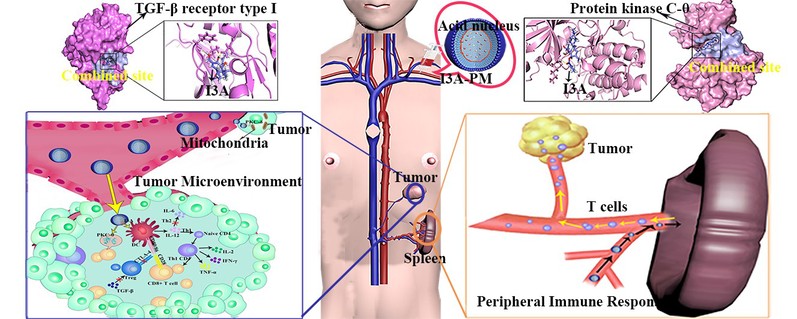
基于上述背景,王成副教授团队采用纳米技术解决I3A水溶性问题,并且递送系统的醇羟基(-CH(CH3)-OH)组成的“酸核”为I3A提供了完美的pH环境(2.5<pH<4.0),解决其pH-不稳定性等问题。课题组通过构建小鼠S180肉瘤模型来对I3A-PM全身给药后的抗肿瘤进行研究,发现I3A-PM具有显著的抗肿瘤效果。一次给药后,抑瘤效果能够持续9天,最高抑瘤率达80.25%。除此之外,I3A-PM免疫刺激效果显著,可以介导Th1免疫,促进IL-12, IL-2, TNF-α,TFN-γ等Th1型细胞因子分泌,显著提高CD4+ T细胞和CD8+T细胞的水平以及CD4/CD8的比例。同时,I3A-PM成功下调具有免疫抑制能力的Treg细胞,和Th2型细胞因子IL-6;通过计算机模拟寻靶技术,发现I3A与免疫抑制性因子TGF-β下游的TGF-β受体I具有高度亲和性,并通过Western Bolt得到了确证。通过纳米技术解决小分子药物疏水性问题,通过EPR效应提高其在病灶部位的聚集,通过肿瘤免疫激活技术“放大靶标”,同时“剿灭”逃逸入血的癌性细胞,为安全有效的抗肿瘤靶向给药系统的设计提供一种新思路和方法。
该研究成果发表于药剂学领域国际知名期刊《Journal of Controlled release》(药物递送领域Top期刊,药学1区,IF=7.9)上。
中国海洋大学医药学院硕士研究生于冕为论文第一作者,山东大学附属省立医院赵苗青博士为并列第一作者,山东大学附属省立医院夏明教授和王成副教授为共同通讯作者。于日磊副教授、初鑫硕士研究生及本科生徐嘉昊为合作作者。同时感谢山东省生物药物研究院邵华荣博士,青岛海洋生物医药研究院曲显俊教授、高江明老师在此工作中给予的帮助,研究工作获得了国家自然科学基金、中央高校基本科研业务费专项等项目的资助。
原文: https://www.sciencedirect.com/science/article/pii/S016836591930255X
Journal of Controlled Release ( IF 7.877 ) Pub Date : 2019-05-06 , DOI: 10.1016/j.jconrel.2019.05.007
【关闭】





